* Данная работа не является научным трудом, не является выпускной квалификационной работой и представляет собой результат обработки, структурирования и форматирования собранной информации, предназначенной для использования в качестве источника материала при самостоятельной подготовки учебных работ.
Современные тенденции в лечении шизофрении. Место эглонила при терапии острых и хронических психозов
Лечение шизофрении является одной из важнейших задач современной психофармакологии, что обусловлено как ее высокой распространенностью в популяции, так и большой частотой инвалидизации пациентов, определяющей то значительное бремя расходов, которое ложится на общество в связи с этим заболеванием. Безусловно, начало психофармакологической эры в начале 50-х годов, открытие хлорпромазина и других нейролептиков революционализировало лечение больных шизофренией. До этого невозможно было себе представить, чтобы какие-либо лекарства могли воздействовать на бред или галлюцинации. Развитие нейролептической терапии привело к созданию психобиологического определения нейролептика, сформулированного еще на заре психофармакологической эры в 1957 г. французскими исследователями J.Delay и P.Deniker. Они выдвинули пять признаков, определяющих препарат нейролептического действия:
1) психолептическое действие без снотворного влияния;
2) купирование различных состояний психомоторного возбуждения;
3) способность редуцировать некоторые психозы (антипсихотическое действие);
4) способность вызывать характерные неврологические и нейровегетативные реакции;
5) преимущественное воздействие на подкорковые структуры мозга.
Наиболее важными из них, на которых я хотел бы сейчас остановиться, являются собственно антипсихотическое действие (способность редуцировать психоз) и способность вызывать характерные экстрапирамидные реакции. J.Delay и P.Deniker считали, что между этими двумя эффектами существует корреляция. В частности, в связи с этим был создан мажептил, который был заказан клиницистами как препарат с наибольшим неврологическим влиянием и который оказался действительно мощным или, по определению французских авторов, инцизивным антипсихотиком.
Таблица 1. Примерная доза некоторых нейролептиков, вызывающая дистонические экстрапирамидные побочные эффекты (по экспериментальным данным, у обезьян)
|
Препарат |
Примерная доза, вызывающая дистоническую реакцию, мг/сут |
Клиническая доза, мг/сут |
|
Галоперидол |
5-20 |
5-20 |
|
Сульпирид |
2000-8000 |
6-1800 |
|
Рисперидон |
5-20 |
4-8 |
|
Сертиндол |
100-400 |
16-30 |
|
Клозапин |
<1500> |
100-800 |
|
Оланзапин |
24-96 |
10-30 |
|
Сероквел |
1200-4800 |
300-900 |
|
Gerlach S., Peacock L. (1995) |
Таблица 2. Дозы и аминазиновые эквиваленты
|
Нейролептик |
Седативное действие |
Антипсихотическое действие |
Аминазиновый эквивалент(условн. ед.) |
Средняя суточная доза |
Суточные дозы, применяемые в стационаре |
|
Хлорпромазин (аминазин) |
++++ |
++ |
1,0 |
300 |
200-1000 |
|
Левопромазин (тизерцин) |
++++ |
+ |
1,6 |
200 |
100-600 |
|
Клозапин (лепонекс, азалептин) |
++++ |
+++ |
1,0 |
300 |
100-900 |
|
Хлорпротиксен (труксал) |
+++ |
+ |
1,5 |
200 |
50-600 |
|
Перициазин (неулептил) |
+++ |
+ |
5,0 |
60 |
300-100 |
|
Поксапин (покситан) |
+++ |
++ |
4,0 |
75 |
200-250 |
|
Промазин (пропазин) |
+++ |
+ |
1,0 |
300 |
100-800 |
|
Зуклопентиксол (цисординол, клопиксол) |
+++ |
++ |
4,0 |
75 |
25-150 |
|
Климемазин (терален) |
++ |
+ |
3,0 |
100 |
25-40 |
|
Перфеназин (этаперазин, трилафон) |
++ |
++ |
6,0 |
50 |
20-100 |
|
Трифлуоперазин (трифтазин, стелазин) |
++ |
+++ |
6,0 |
50 |
20-100 |
|
Галоперидол (галдол) |
++ |
+++ |
30,0 |
10 |
6-100 |
|
Молиндол (мобан) |
++ |
+++ |
3,0 |
100 |
50-250 |
|
Зипразидон |
++ |
++ |
3,0 |
100 |
80-160 |
|
Сультоприд (барнетил, топрал) |
++ |
+++ |
0,5 |
600 |
200-1200 |
|
Бенперидол (френактил) |
++ |
+++ |
40,0 |
6 |
2-14 |
|
Флупентиксол (флуанксол) |
++ |
+++ |
20,0 |
12 |
3-18 |
|
Трифлуоперидол (триседил) |
++ |
++++ |
40,0 |
5 |
1-15 |
|
Дроперидол (дролептан) |
++ |
++++ |
50,0 |
4 |
2-40 |
|
Кветиапин (сероквел) |
++ |
++ |
1,0 |
400 |
75-750 |
|
Рисперидон (риспердал, рисполепт) |
++ |
++ |
35,0 |
6-8 |
4-12 |
|
Зотепин (лодопин) |
++ |
++ |
1,0 |
300 |
100-600 |
|
Прохлорперазин (метеразин) |
+ |
++ |
3,0 |
100 |
75-200 |
|
Флуфеназин (модитен, фторфеназин) |
+ |
+++ |
35,0 |
8 |
2-20 |
|
Пимозид (орал) |
+ |
++ |
35,0 |
8 |
2-20 |
|
Пипотиазин (пипортил) |
+ |
+++ |
7,0 |
40 |
30-120 |
|
Тиопроперазин (мажептил) |
+ |
++++ |
15,0 |
20 |
5-60 |
|
Оланзапин (зипрекса) |
+ |
+++ |
15,0 |
20 |
10-30 |
|
Сертиндол (сердолект) |
+ |
+ |
20,0 |
12 |
8-24 |
|
Метофеназин (френолон) |
+ |
++ |
7,5 |
40 |
10-100 |
|
Тиаприд (тиапридаль) |
+ |
+ |
1,0 |
300 |
200-600 |
|
Сульпирид (эглонил) |
— |
++ |
0,5 |
600 |
400-2000 |
|
Амисульпирид (солиан) |
— |
++ |
1,0 |
300 |
200-600 |
|
Карбидин |
— |
+ |
3,0 |
100 |
50-200 |
|
Карпипрамин (празинил, дефектон) |
— |
++ |
3,0 |
100 |
50-200 |
Рис. 1. Бимодальное распределение оценок глобальной эффективности эглонила (сульпирид) у больных шизофренией в зависимости от максимальной суточной дозы (n=36)
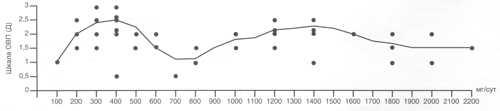
Таблица 3. Синдромы-мишени действия сульпирида (эглонила) у больных шизофренией — I
|
Диапазон суточных доз, мг |
||
|
Депрессивные состояния |
— постпсихотическая (постшизофреническая) депрессия |
200-400 |
|
и депрессивно-бредовые |
— депрессивно-параноидные состояния |
|
|
— депрессивно-ипохондрические |
||
|
— деперсонализационные |
||
|
— астено-анергические |
||
|
Дефицитарные состояния |
— апато-абулические |
200-400 |
|
(негативная симптоматика) |
— эмоциональная нивелировка |
|
|
— аутизм, социальная изоляция |
||
|
— когнитивные нарушения |
||
|
— психомоторные нарушения (манерность, кататоническая симптоматика) |
Таблица 4. Синдромы-мишени действия сульпирида (эглонила) у больных шизофренией — II
|
Диапазон суточных доз, мг |
||
|
Параноидные (галлюцинаторно-бредовые) |
— параноидальный (ипохондрический) |
1200-1800 |
|
— галлюцинаторно-параноидный |
||
|
— параноидный (персекуторный) |
||
|
— парафренный |
||
|
Острые бредовые (шизоэффективные) |
— острый бредовый |
800-1400 |
|
— депрессивно-параноидный |
||
|
— онейроидно-кататонический |
||
|
Гиперкинетический |
— поздние дискинезии |
200-600 |
Таблица 5. Феноменологическое сходство некоторых клинических синдромов с негативными расстройствами при шизофрении
|
Негативные симптомы |
Депрессия |
Побочное действие нейролептиков |
|
Эмоциональное уплощение |
Ангедония, психическое безразличие, анестезия |
Психическая индифферентность, амимия |
|
Апато-абулические нарушения (снижение психоэнергетического потенциала) |
Моторная заторможенность |
Акинезия, повышение мышечного тонуса |
|
Когнитивные нарушения, бедность речи и ассоциативного мышления |
Идеаторная заторможенность, трудности в сосредоточении внимания |
Брадипсихизм, когнитивные расстройства, снижение вигилитета, нарушение концентрации внимания, затруднение речевой продукции |
|
Аутизм |
Социальная самоизоляция |
Вынужденное ограничение социальных контактов |
Рис. 2
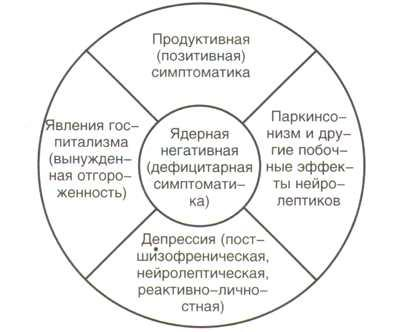
Таблица 6. Нежелательные эффекты при лечении эглонилом 2851 больных, страдающих шизофренией, эндогенной или невротической депрессией
(Альбертс и соавт. Исследование побочных эффектов у пациентов, лечившихся догматилом. Sem. Hop. 1985; 60:1351-7)
|
Нежелательные эффекты |
Число больных |
|
|
абс. |
% |
|
|
Неврологические |
||
|
— тремор |
147 |
5 |
|
— ригидность |
125 |
4 |
|
— акатизия |
66 |
2 |
|
— острая дистония |
46 |
2 |
|
— саливация |
17 |
1 |
|
Психиатрические |
||
|
— тревога |
86 |
3 |
|
— раздражительность |
87 |
3 |
|
— колебания настроения |
18 |
1 |
Таблица 7. Нежелательные эффекты при лечении эглонилом 2851 больных, страдающих шизофренией, эндогенной или невротической депрессией
|
Нежелательные эффекты |
Число больных |
|
|
абс. |
% |
|
|
Вегетативные |
||
|
— сухость во рту |
55 |
2 |
|
— головокружение |
49 |
2 |
|
— потливость |
23 |
1 |
|
Сердечно-сосудистые |
||
|
— гипотензия |
24 |
1 |
|
Эндокринные |
||
|
— аменорея |
27 |
1 |
|
— галакторея |
23 |
1 |
|
Прочие |
||
|
— гастроинтестинальные |
120 |
4 |
|
— увеличение массы тела |
79 |
3 |
Таблица 8. Идеальный нейролептик
-
Более широкий спектр биохимического и клинического действия
-
Одновременная эффективность при различных синдромальных
-
вариантах и стадиях течения шизофрении
-
купирование психомоторного возбуждения
-
и галлюцинаторно-бредовой симптоматики при поддержании
-
нормального уровня бодрствования больных
-
Коррекция негативной симптоматики
-
Возможность длительного применения без развития явлений
-
адаптации
-
Возможность назначения 1 раз в день или реже
-
(для пролонгированных форм)
-
Хорошая переносимость (отсутствие экстрапирамидных
-
и других соматоневрологических побочных эффектов)
-
Минимальное число лекарственных взаимодействий
После введения в практику различных групп фенотиазинов в 1958 г. появился первый бутирофеноновый нейролептик галоперидол, а затем в 1966 г. — родоначальник группы бензамидов сульпирид (эглонил).
Хочу обратить внимание на то, что уже на протяжении более чем 30 лет эглонил успешно применяется в психиатрической практике. В 1968 г. началась эра “атипичных нейролептиков”, как их теперь называют, к которым относятся клозапин, зотепин, рисполепт и другие препараты. Основной чертой атипичных нейролептиков является малая выраженность или отсутствие экстрапирамидных побочных эффектов. Именно в силу этого было подвергнуто ревизии психобиологическое определение нейролептиков J.Delay и P.Deniker (1957).
Вместе с тем если рассматривать этот вопрос более детально, то в целом определение остается верным. Все дело в том, что ученым удалось «развести» дозы препаратов, вызывающие экстрапирамидный побочный эффект и собственно антипсихотическое действие. Экспериментальные данные S.Gerlach, L.Peacock (1995), полученные на макаке-резус, позволяют судить о клинической дозе, вызывающей антипсихотический эффект, и примерной дозе, вызывающей дистоническую экстрапирамидную реакцию ( табл. 1 ).
Для классического бутерофенона — галоперидола эти диапазоны доз приблизительно одинаковы, т.е антипсихотический эффект всегда сопровождается экстрапирамидной симптоматикой той или иной степени выраженности. Для антипсихотиков нового поколения эти диапазоны доз как бы «перекрываются». Например, 4-6 мг рисполепта — достаточно эффективная доза для купирования практически любых психотических состояний, в то время как экстрапирамидные побочные эффекты развиваются при превышении этой дозы. Именно поэтому в свое время фирма скорригировала терапевтическую дозу препарата в сторону ее понижения до 6-8 мг. То же самое касается и других современных нейролептиков. Примечательно, что для сульпирида клинически эффективная доза варьирует очень широко от 600 до 1800 мг, а доза, при которой возникает выраженная дистоническая реакция, превышает 2 г. В широком смысле по этому показателю сульпирид может быть отнесен к атипичным нейролептикам.
Бензамидная моноциклическая структура является облигатным фрагментом всех нейролептиков. Для химической классификации нейролептиков большее значение имеет стереохимическая структура молекулы, и в соответствии с этим сейчас выделяют ряд основных групп препаратов. Это фенотиазины, бутирофеноны, бензамиды. К последним относятся сульпирид (эглонил), сультоприд (топрал или барнетил), тиаприд (тиапридал), метоклопрамин (реглан), практически не применяемый в психиатрической практике, но хорошо известный в гастроэнтерологии, новый представитель группы бензамидов — амисульприд или сольян, который уже зарегистрирован в Европе, но пока еще не вошел в практику в России, и некоторые другие.
Важнейшее значение для реализации антипсихотического эффекта действия и экстрапирамидных побочных явлений имеет значение блокада D2 дофаминовых рецепторов в нигростриальных и лимбической областях мозга. К вероятным клиническим проявлениям такой блокады относятся антипсихотическое и седативное действия, экстрапирамидные явления, а также усиление выработки гормона пролактина и как следствие галакторея, нарушения менструального цикла, нарушения водного обмена, остеопороз и некоторые другие эффекты, связанные с воздействием на туберинфондибулярную систему, а также развитие феномена гиперчувствительности и малокурабельных поздних дискинезий при длительной блокаде D2-рецепторов.
Из пяти выделенных в настоящее время дофаминовых рецепторов первые два типа являются постсинаптическими. Блокада этих рецепторов прерывает дофаминергическую передачу в синапсе. В то же время существуют подтипы этих рецепторов и на пресинаптической мембране, взаимодействие с которыми оказывает прямо противоположный — стимулирующий (дезингибирующий эффект), развивающийся вследствие выхода в клеточную мембрану дофамина, с чем ученые связывают наличие у некоторых препаратов, особенно при применении в малых дозах, так называемого психостимулирующего действия.
Современные методы исследования (например, техника связывания радиоизотопных лигандов) позволили практически полностью определить степень связывания нейролептика с различными рецепторами не только дофаминовыми, но и другими. Все нейролептики в соответствии с их влиянием на дофаминовые рецепторы можно разделить на пять групп. В первую группу попадают препараты, блокирующие D2-рецепторы и практически не действующие на другие типы. Клинически это проявляется прежде всего антипсихотическим действием и при применении препарата в малых дозах, стимулирующим, связанным с воздействием и на пресинаптические рецепторы, а также отсутствием серьезных адренолитических и холинолитических побочных эффектов.
Переходя к клиническим воззрениям на антипсихотическое действие нейролептиков, следует обратиться к концепции Г.Я. Авруцкого о спектре клинической активности нейролептика, которая остается актуальной и сегодня. Она включает в себя семь параметров:
1. Глобальное антипсихотическое или “инцизивное” действие.
2. Первичное седативное (затормаживающее) действие.
3. Избирательное или селективное антипсихотическое действие.
4. Активирующее (растормаживающее), дезингибирующее и антиаутистическое антипсихотическое действие.
5. Депрессогенное действие.
6. Нейротропное действие.
7. Соматотропное действие.
Рассматривая три из этих параметров: глобальное антипсихотическое (инцизивное) действие, первичное седативное действие (затормаживающее) и активирующее (растормаживающее, дезингибирующее или антиаутистическое) действие, следует обратиться к биполярной классификации нейролептиков P.-A.Lamber и E.Revol (1966), представленной в табл. 2 . Французские авторы расположили все нейролептики в порядке убывания седативного эффекта и нарастания растормаживающего (дезингибирующего) и антипсихотического действия. В соответствии с этой классификацией препараты седативной группы, к которым относятся хлорпромазин, аминазин, клозапин и др., независимо от дозы вызывают седативный эффект. При нарастании антипсихотического действия, особенно при применении малых доз, клинически проявляется дезингибирующее (растормаживающее) действие нейролептика, которое связано с воздействием небольших доз на рецепторы пресинаптической мембраны, вследствие чего происходит некоторая дофаминергическая стимуляция.
К дезингибирующим нейролептикам можно отнести много препаратов, но в настоящее время на нашем рынке остался только сульпирид. Эффективность эглонила в свете теоретических воззрений на зависимость клинического эффекта от применяемой дозы была проанализирована на материале наших предшествующих исследований. Как видно из рис. 1 , в распределении оценок глобальной эффективности (по шкале Авруцкого, Зайцева “Оценка общей выраженности психоза — ОВП”) эглонила у больных шизофренией в зависимости от максимальной суточной дозы обращает на себя внимание прежде всего его бимодальность, т.е. максимальный терапевтический эффект наблюдался в интервале доз 200-400 мг/сут. При применении доз выше 500 мг/сут наблюдался некоторый “провал”, и эффективность вновь нарастала при использовании дозы 1200-1400 мг/сут. Этот эффект очень интересен, так как других нейролептиков с таким бимодальным распределением неизвестно. Обычно эффективность нарастает плавно вместе с дозой. Анализ случаев, в которых имела место эффективность в этих диапазонах доз, показал, что в первый пик (дозы 200-400 мг) попали два рода состояний (табл. 3 ) — депрессивные и депрессивно-бредовые, т.е. связанные с гипотимным аффектом, и состояния с преобладанием негативной симптоматики — аутистические, эмоциональные расстройства, когнитивные нарушения, а также кататоническая симптоматика, которая также вошла в этот кластер дефицитарных синдромов. Второй пик (дозы 600-1800 мг/сут) приходился собственно на бредовые психозы (табл. 4 ).
Было выделено два вида состояний, т.е. параноидные галлюцинаторно-бредовые психозы, объединяющие разные синдромы: и парафренный, и персикуторный, и галлюцинаторно-бредовой, и паранояльный (в основном ипохондрический).
В этих случаях дозы не только приближались к максимальным, но и соблюдалось правило нарастания клинического эффекта с увеличением дозы. В эту группу попали случаи и острых бредовых психозов (по типу шизоаффективных), хотя здесь эффективны были несколько более низкие дозы (800-1400 мг/сут).
При отдельном анализе такого признака, как гиперкинетический синдром, в том числе поздняя дискинезия, было установлено, что эглонил существенно уменьшает выраженность симптоматики, хотя, конечно, и не излечивает полностью.
Исходя из современных воззрений, полученные данные можно трактовать как воздействие на два различных типа шизофрении в соответствии с классификацией Т.Кроу — на негативную и позитивную шизофрению. И действительно, в первом кластере преобладали негативные синдромы, во втором — позитивные.
Противоречивым, на первый взгляд, представляется включение в первый кластер депрессивных расстройств. Из литературы известно, что эглонил обладает некоторыми тимоаналептическими (антидепрессивными) свойствами. Вероятно, речь идет не об истинном тимоаналептическом действии и эффективности при типичных эндогенных депрессиях. В данном случае в настоящем исследовании речь идет о том, что мы не смогли феноменологически четко разграничить эти депрессивные синдромы от негативных расстройств при шизофрении. Из табл. 5 видно, что многие психопатологические феномены депрессивной, негативной и психопатологической симптоматики пересекаются и их очень сложно разделить. По-видимому, речь идет прежде всего о глобальном дезингибирующем или растормаживающем действии малых доз эглонила, в связи с чем он оказался эффективным для коррекции негативной и вторичной депрессивной симптоматики. Думается, что речь идет о коррекции именно вторичных негативных расстройств, не столько собственно дефекта в крепелиновском понимании, как некоего необратимого “рубца”, сколько о вторичной симптоматике. На рис. 2 показано, что ядерная дефицитарная симптоматика составляет меньшую долю негативной симптоматики, большая часть которой связана с развитием психоза, паркинсонизма и депрессии.
Из данных литературы известна достаточно высокая переносимость эглонила. При применении в малых дозах процент развития как психиатрических, так и неврологических побочных эффектов близок к плацебо-эффекту ( табл. 6 ).
Вегетативные и сердечно-сосудистые эффекты также минимальны (табл. 7 ).
Конечно, при нарастании дозы появляются и побочные эффекты, но это касается больше антипсихотического эффекта.
В заключение позвольте проанализировать свойства эглонила в свете концепции идеального нейролептика ( табл. 8 ).
Эглонил не соответствует идельному нейролептику лишь по признаку более широкого биохимического действия, так как он, наоборот, оказывает в большей степени селективное действие в основном на второй тип, а в малых дозах — на третий тип дофаминовых рецепторов. Однако в остальном для него, так же как и для других атипичных нейролептиков, характерна эффективность при различных вариантах и стадиях шизофрении; достаточно типична способность корригировать негативную симптоматику, прежде всего вторичную; возможность длительного применения с профилактической или противорецидивной целью без развития явлений адаптации; хорошая переносимость. Отдельно следует подчеркнуть отсутствие риска серьезных лекарственных взаимодействий с эглонилом. Его фармакокинетическое действие не связано с ферментативной системой печени, эглонил выводится почками, что изначально предполагает отсутствие взаимодействий через систему цитохромов P450.
Статья С.Н. Мосолова «Современные тенденции в лечении шизофрении. Место эглонила при терапии острых и хронических психозов»
