Сахарный диабет у детей. Этиология, патогенез, клиническая картина, диагностика и дифференциальная диагностика, принципы лечения
Впервые сахарный диабет (СД) описан в древней Индии более 2000 лет назад.
СД — синдром хронической гипергликемии, развивающийся вследствие абсолютной (I тип) или относительной (II тип) недостаточности инсулина и проявляющийся глюкозурией, полиурией, полидипсией, нарушениями липидного (гиперлипидемия, дислипидемия), белкового (диспротеинемия) и минерального обмена (гипокалиемия), с развитием осложнений.
Инсулинзависимый СД (ИЗСД, I типа), Инсулиннезависимый СД (ИНЗСД, II типа), Частота и возрастная структура СД
В последние десятилетия частота СД неуклонно увеличивается, число больных в развитых странах составляет до 5% от общей популяции, в действительности распространенность СД выше, так как не учитываются его латентные формы (еще 5% от общей популяции).
Дети и подростки до 16 лет составляют 5-10% всех больных диабетом. СД проявляется в любом возрасте (существует даже врожденный диабет), но наиболее часто в периоды интенсивного роста (4-6 лет, 8-12 лет, пубертатный период).
Дети грудного возраста поражаются в 0,5% случаев. СД чаще выявляется в возрасте от 4 до 10 лет, в осенне-зимний период.
Самая высокая частота СД у детей (в возрасте до 15 лет) отмечается в Скандинавских странах (в Финляндии 40:100.000 населения).
В Средней Азии заболеваемость среди детей СД в 4 раза ниже, чем в России (6,4:100000) (Ю.А. Князев, 1991).
В Кыргызстане на 1998 год заболеваемость СД была 7,9:100.000 против 64,3:100.000 в Эстонии.
Для детей и подростков СД имеет более тяжелое течение, компенсация болезни труднее, что обусловлено напряженностью обменных процессов, обеспечивающих интенсивный рост ребенка, и повышенной потребностью в анаболических гормонах (в т. ч. инсулине).
При более высокой потребности в инсулине у детей имеется значительный дефицит гормона, что способствует возникновению тяжелого варианта СД у детей.
С другой стороны, в детском и юношеском возрасте имеется более высокий уровень основных контринсуллярных гормонов (СТГ, ТТТ, АКТТ, ГКС), ответственных за анаболические процессы, а в пубертатном периоде повышается лабильность ЦНС и симпатической НС, приводящей к повышенному выбросу адреналина (контринсулярный гормон).
Понятие о типах СД и механизмах их развития
ВОЗ выделяет два основных типа — ИЗСД (I тип) и ИНЗСД (II тип).
Сахарный диабет первого типа у детей
... увеличивают вероятность заболевания, но диабет 1 типа встречается гораздо реже, чем диабет 2 типа. Лечение сахарного диабета 1 типа у детей Лечение диабета 1 типа у детей почти всегда включает компенсаторные ... у детей сахарный диабет гипотиреоз дети Гипотиреоз у детей может быть врожденным или приобретенным. При врожденном гипотиреозе малыши рождаются с недостаточностью щитовидной железы. Частота ...
I тип составляет около 12-15% всех заболевших и почти 100% заболевших в детском возрасте.
Клинически ИЗСД характеризуется бурной манифестацией типичных симптомов СД с развитием кетоацидоза (иногда уже через 2-4 недели после начала заболевания).
ИНЗСД развивается постепенно, исподволь, течение торпидное (медленное), остается незамеченным долго, иногда выявляется случайно или активно как углеводная интолерантность. При манифестации компенсация метаболических нарушений с помощью патогенетической терапии трудна (иногда невозможна), так как уже имеются глубокие нарушения липидного обмена, двухсторонняя диабетическая катаракта и полисистемная ангиопатия с артериолосклерозом.
Этиология СД
Причина полностью не выяснена. Имеется наследственная предрасположенность, передающаяся по аутосомно-рецессивному (родители внешне здоровы), реже — по аутосомно-доминантному типу (один или оба родителя больны).
Установлено, что при больных СД родителях дети имеют риск заболевания до 100%, а при болезни одного из них — до 85%, одного из прародителей — до 60%.
Теория о полигенном
СД предполагает участие следующих факторов:
- синтез патологического проинсулина и биологически неактивного инсулина;
- нарушение кровоснабжения бета-клеток;
- патология глюкорецепторов бета-клеток;
- наличие в организме аномальных форм инсулина.
Факторы, обуславливающие наследование СД неоднородны, имеется связь между различными проявлениями ИЗСД и системой НЛА (антигенов 6-й хромосомы).
У носителей антигенов В8, В15, ДDRЗ, DR4 заболеваемость ИЗСД в 10-20 раз выше, чем у остальной популяции. У носителей НLА-антигенов В15, ДR4 ИЗСД развивается в младшем возрасте после перенесенной вирусной инфекции, а носители В8 и ДRЗ заболевают в более старшем возрасте при повреждении ПЖ аутоиммунного характера.
Установлена повышенная частота сочетания ИЗСД с другими эндокринопатиями аутоиммунного характера (щитовидной железы и надпочечников), при этом выявляются антитела к островкам Лангерганса, субклеточным компонентам щитовидной железы и тканям надпочечников.
Таким образом, ИЗСД носит характер аутоиммунного инсулинита, выработка аутоантител к ткани островков Лангерганса генетически обусловлена, что подтверждает связь между временем развития ИЗСД и комбинациями НLА-антигенов. ИНЗСД связи с антигенами НLА-системы не имеет, хотя наследственная предрасположенность выявляется.
Экзогенные факторы
— Вирусные инфекции. Тропность к инсулярному аппарату имеют вирусы Коксаки В4, эпидемического паротита, краснухи, инфекционного гепатита, гриппа, инфекционного мононуклеоза, цитомегалии, ветряной оспы (вызывают инсулит с формированием аутоиммунного процесса).
- Стрессовые ситуации — травмы, испуг, тяжелые эмоциональные переживания, физическая и умственная перегрузка. При стрессе повышается уровень АКТГ, СТГ, тиреоидных гормонов, ГКС, катехоламинов, глюкагона, что подавляет инсулярный аппарат.
— Переедание углеводистой и жирной пищи требует, с одной стороны напряженной работы инсуллярного аппарата по утилизации громадных количеств поступающей извне глюкозы, с другой — ведет к развитию ожирения с жировой инфильтрацией инсулин чувствительных периферических тканей (требуется все больше инсулина, а жировое перерождение приводит к резистентности тканей к инсулину и относительной инсулиновой недостаточности).
Аутоиммунные заболевания
... ёртую группу включены заболевания, которые основаны на нарушениях функции лимфоидной ткани. В этом случае появляются клетки, разрушающие здоровые ткани организма. С учетом огромного разнообразия аутоиммунных заболеваний, а также их ... дерматомиозит чаще всего встречаются у взрослых людей в возрасте от 40 до 60 лет, а также у детей от 5 до 15 лет. У женщин вероятность развития этих ...
- Лечение контринсуллярными гормонами с развитием транзиторного стероидного или тиреоидного диабета, который при генетической предрасположенности может трансформироваться в истинной. Иммунизация лиц с предрасположенностью к диабету приводит к аутоиммунному ответу с поражением бета-клеток. Иммунологический процесс, приводящий в итоге к СД I типа, начинается за годы до появления клинических симптомов заболевания. Во время этого преддиабетического периода в крови у пациентов можно обнаружить повышенные титры различных аутоантител к островковым клеткам (ICA) и инсулину (IAA), к белку, найденному в островковых клетках, к GAD (глютаматдекарбоксилазе).
Было доказано, что если уровень ICA значительно повышен (>20 JDF единиц), то риск развития СД I типа в течение последующих 5-7 лет составляет 40-60%.
Таким образом, при развитии СД имеет место сочетание генетических и внешних факторов. Кроме дефектов иммунитета (НLА), предполагаются также дефекты определенных локусов на коротком плече 6-й хромосомы, приводящей к изменению мембранных белков бета-клеток (они становятся менее устойчивыми к повреждающим факторам).
Редкой причиной СД у детей раннего возраста является врожденная гипоплазия ПЖ со снижением экзо- и эндокринных функций.
Патогенез СД у детей
В патогенезе ИЗСД основную роль играют следующие механизмы, приводящие к гормональной недостаточности бета-клеток (первично-генетические дефекты):
- Врожденное нарушение рибосомного аппарата бета-клеток, ответственного за накопление гранул инсулина в цитоплазматической сети.
- Дефицит аминокислот, необходимых для синтеза инсулина.
- Нарушение образования инсулина из предшественников и выделения его в кровь.
- Нарушение электролитного обмена в бета-клетках.
- Угнетение системы циклической 3,5-АМФ в бета-клетках, активирующей окислительный гликолиз (источник питания бета-клеток).
При ИНЗСД ПЖ и объем секретируемого инсулина не изменены. Важными в его развитии являются следующие механизмы: 1. Снижение или отсутствие первой фазы секреции инсулина (при повышении глюкозы в крови отмечается двухфазность секреции инсулина — первоначальный выброс связан с ранее накопленным в бета-клетках инсулином, а вторичное — с выделением вновь образованного инсулина).
2. Ферментативные дефекты на уровне периферических действий инсулина (уменьшение числа рецепторов к инсулину и снижение чувствительности к нему периферических тканей).
3. Дефекты инсулинового биогенеза. 4. Дефицит ионов цинка, необходимых для полимеризации молекулы инсулина и накопления его в гранулах бета-клеток. 5. Образование антител к инсулину. 6. Присутствие в крови антагонистов инсулина. 7. Нарушение способности жировой ткани расщеплять связанный инсулин. 8. Извращенная реакция тканей к циркулирующей форме инсулина. 9. Периферическая инактивация инсулина.
ИЗСД у детей развивается в результате аутоиммунного инсулината, приводящего к деструкции бета-клеток и хронической латентно протекающей гипергликемии. В.Л. Лисс (1993) выделяет 6 стадий развития ИЗСД:
Заболевания крови у детей
... заболеваний крови у детей. Для достижения поставленной цели мне предстоит решить следующие задачи: 1. Дать характеристику наиболее часто встречающихся заболеваний крови у детей; 2. Раскрыть особенности сестринского ухода при каждом заболевании крови; ... 2. Недостаточное поступление в кроветворные органы веществ (железо, витамин В12, ... боли в левой половине грудной клетки и повышение температуры тела ( ...
- Стадия генетической предрасположенности (потенциальный ИЗСД).
В этой стадии нет ни аутоиммунных, не биохимических нарушений, диагностируется она по наличию антигенов высокого риска системы НЛА, но реализуется далеко не у всех.
- Воздействие провоцирующих факторов, которые предположительно вызывают развитие активного аутоиммунного инсулинита.
— Стадия хронического аутоиммунного инсулинита (у 90% больных определяются антитела к поверхностному антигену бета-клеток, их цитоплазматическим компонентам, антиинсулиновые антитела, повышается количество активированных Т-лимфоцитов).
Первоначально секреция инсулина не нарушена, сохраняется нормогликемия.
- В результате деструкции бета-клеток отмечается снижение инсулина в ответ на введение глюкозы при сохранении нормогликемии натощак — стадия латентного СД, с нарушением толерантности к углеводам (диагностируется редко).
- Явный ИЗСД, клиническая манифестация заболевания, развивается остро при гибели 80-90% бета-клеток, при этом сохраняется остаточная секреция инсулина.
- Полная деструкция бета-клеток и абсолютная инсулиновая недостаточность.
Углеводный обмен
Инсулин обеспечивает проницаемость клеточных мембран для глюкозы путем соединения со специфическими рецепторами. Активирует внутриклеточные энзимные системы (гексокиназы), обеспечивающих метаболизм глюкозы, процесс фосфорилирования глюкозы в клетке, действуя на глюкокиназу (превращает глюкозу в Г-6-Ф) и угнетает активность Г-6-Фазы (превращает Г-6-Ф в глюкозу).
гликогенолиз
Усиливает образование ацетил-СоА, необходимого для дальнейшего синтеза липидов, холестерина, свободных жирных кислот и кетоновых тел, стимулирует синтез энергетического соединения АТФ и усиливает образование восстановленного НАДФ-Н 2 , необходимого для синтеза жирных кислот.
гипергликемии
Жировой обмен
Интенсивность липогенеза в организме прямо пропорциональна интенсивности процессов утилизации глюкозы, которые идут под контролем инсулина и сопровождается образованием ацетил-Со-2а и НАДФ-Н 2 , участвующих в синтезе свободных жирных кислот — исходного материала для синтеза триглицеридов жировой и мышечной ткани. Кроме того, образующийся при гликолизе альфа-глицерофосфат стимулирует эстерификацию СЖК.
Таким образом, инсулин стимулирует липогенез и оказывает антилиполитический эффект (внутри липоцитов тормозит аденилатциклазу, снижает уровень ЦАМФ липоцитов, необходимого для процессов липолиза).
Недостаток инсулина вызывает усиление липолиза (расщепление триглицеридов до СЖК в адипоцитах).
СЖК в повышенном количестве поступают в кровь, а оттуда — в печень, где происходит их использование по двум путям:
- Ресинтез триглицеридов, что выражается в жировой инфильтрации печени с увеличением ее размеров.
- Распад СЖК с образованием кетоновых тел (ацетоуксусная, бета-оксимасляная кислоты и ацетон).
Белковый обмен
В присутствии инсулина в жировой и мышечной ткани происходит синтез белка. Инсулин ускоряет прохождение аминокислот в клетки, способствует включению их в пептидные цепи в клеточном рибосомном аппарате. Распад (катаболизм) белков под влиянием инсулина тормозится.
Недостаточность инсулина вызывает повышенный катаболизм белков мышечный ткани (компенсация дефицита энергии при неполном использовании глюкозы) и накопление в крови азотсодержащих продуктов — аминокислот (идут в печень, где используется в процессе глюконеогенеза), мочевины, мочевой кислоты, аммиака. В результате потери жидкости, электролитов, усиления липолиза и протеолиза, потери гликогена, масса тела снижается (похудение), возникает мышечная слабость, трофические нарушения кожи и слизистых оболочек.
Патогенез коматозных состояний при СД у детей
Кома (греч. «сон») характеризуется нарушением сознания, отсутствием психической деятельности, нарушением двигательных, чувствительных и соматовегетативных функции организма (В.А. Михельсон).
У детей СД протекает более лабильно, бурно, с большей выраженностью кетоацидоза и жировой инфильтрации печени и чаще возникают коматозные состояния. Развитие комы могут провоцировать инфекционные заболевания, оперативные вмешательства, грубые нарушения режима и диеты, поздняя диагностика, неправильное лечение и стрессовые воздействия (травмы, психические надрывы).
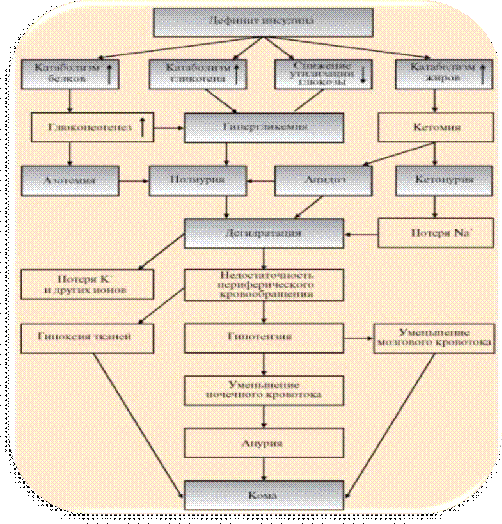
В зависимости от патогенеза различают следующие виды ком при СД у детей:
- Кетоацидотическая (собственно диабетическая) кома.
- Гиперосмолярная кома.
- Гиперлактацидемическая (молочнокислая) кома.
- Первично-церебральная кома.
- Гипогликемическая кома.
Кетоацидотическая кома. Недостаток инсулина приводит к усилению липолиза и повышение в крови концентрации СЖК, поступающих в печень, где часть из них подвергается дальнейшему распаду с образованием кетоновых тел (КТ) — ацетоуксусной, бета-оксимасляной кислот и ацетона. КТ — источник питания инсулинзависимых тканей (мышечной, жировой) в условиях инсулиновой недостаточности. При этом, несмотря на хорошее использование КТ тканями, полного их сгорания из-за очень интенсивного кетогенеза не происходит и они накапливаются в крови (кетоз, чреватый токсическим эффектом).
Избыток КТ выводится с мочой (кетонурия) и выдыхаемым воздухом (запах ацетона), однако их накопление превалирует над выведением и в дальнейшем развивается диабетический кетоацидоз (ДКА) с гипервентиляцией и активизацией гликолиза в тканях. При этом гликолиз идет с накоплением недоокисленных продуктов (пировиноградной и молочной кислот), что ведет к развитию метаболического ацидоза.
В патогенезе ДКА и кетоацидотической комы играют роль 4 основных процесса:
— Активизация неогликогенеза и последующего гликолиза образовавшейся из белков и жиров глюкозы в условиях дефицита инсулина и торможения гексокиназы приводит к накоплению в тканях пировиноградной и молочной кислоты. Одновременно в крови накапливаются КТ, токсически влияющие на ткани головного мозга. Накопление недоокисленных продуктов обмена и КТ приведет к развитию метаболического ацидоза.
— Гипергликемия и гиперкетонемия увеличивают осмолярность крови и внеклеточной жидкости, что ведет к дегидратации клеток и усиленному осмотическому диурезу с потерей жидкости и электролитов и сгущению крови. Особенно важна потеря Р, отражающаяся на содержании 2,3-дифосфоглицерата, влияющего на кислород- связывающие свойства гемоглобина. При ДКА и повышенной фосфоурии уровень дифосфоглицерата снижается, увеличивается уровень глюкогемоглобина, обладающего большим сродством к кислороду и затрудняющего отдачу кислорода тканям — развивается тканевая гипоксия.
- Усиление катаболизма тканевых белков ведет к накоплению в крови азотсодержащих продуктов — аминокислот, аммиака, мочевой кислоты, мочевины (азотемия).
— Клетки нервной системы, печени, бета-клетки ПЖ, эритроциты относятся к инсулиннезависимым, т.е. проникновение глюкозы в эти клетки происходит без участия инсулина, а по градиенту концентрации глюкозы в крови и клетке. При гипергликемии в нервных клетках накапливается глюкозы больше, чем может фосфорилироваться, затем они превращается в осмотически активные вещества (сорбитол, фруктоза), которые вместе с избыточной концентрацией органических кислот и натрия устремляются внутрь клеток головного мозга (обуславливают высокую гидрофильность тканей, и их предрасположенность к отеку).
Углубление метаболических нарушений при кетоацидотической коме сопровождается расстройством функций всех органов и систем. Из-за гиперкетонемии, метаболического ацидоза и повышенного образования углекислоты наступает гипервентиляция (дыхание Куссмауля).
Вследствие потери жидкости, ацидоза, гипокалиемии и других метаболических сдвигов ослабевает сердечная деятельность, падает артериальное давление, снижается функция почек.
Гиперосмолярная кома
В основе патогенеза предполагается снижение продукции АДГ задней доли гипофиза, что создает условия для повышенной потери жидкости (нет реабсорбции) и гиперосмолярности крови. Отсутствие кетоза объясняется резко выраженной гипергликемией, препятствующей выходу гликогена из печени, в результате чего затрудняется доступ СЖК в печень и уменьшается образование кетоновых тел. Гиперлактацидемическая кома развивается при наличии сопутствующих заболеваний, протекающих с гипоксией и нарушением КЩС, анемией, проявлений ССН при ВПС, бронхолегочных заболеваниях. При инсулиновой недостаточности, ацидозе и гипоксии угнетается аэробный путь окисления глюкозы (нет кислорода и активации гексокиназы) и усиливается анаэробный гликолиз из глюкозы, образовавшейся из белков и жиров при гликонеогенезе, с повышенным образованием пировиноградной и молочной кислот.
Первично-церебральная кома развивается у длительно болеющих СД детей на фоне лечения кетоацидотической гипергликемической комы большими дозами инсулина. Патогенетической ее основной является отек мозга, который связан с:
- Нарушением мозгового кровообращения в результате возбуждения инсулином центров парасимпатической нервной системы.
- Возникновением отека мозга под воздействием инсулина вследствие более быстрого снижения сахара в крови, чем в мозговой ткани
- Интенсивным накоплением под влиянием инсулина и гипергликемии в головном мозге сорбитола и фруктозы, обладающих высокой осмотической активностью.
Гипогликемическая кома развивается при передозировка экзогенного инсулина, недостаточном питании после введения инсулина и лабильном течении диабета (рвота, понос, декомпенсация).
По В.А. Михельсону, гипогликемическая кома развивается при уровне глюкозы в крови у недоношенных новорожденных ниже 1,1ммоль/л, у доношенных новорожденных — ниже 1,7 ммоль/л. Иногда наблюдается и при более высоких цифрах гликемии (при резком уменьшении сахара крови на фоне лечения кетоацидотической комы инсулином возникает симптомокомплекс гипогликемии при уровне сахара, превышающем физиологическую норму).
При гипогликемии, в первую очередь, страдает головной мозг (недостаточное поступление глюкозы к клеткам ЦНС нарушает утилизацию ими кислорода, а углеводное и кислородное голодание сопровождаются развитием в них энергетического дефицита, повреждением ферментных систем, разрушением структурных элементов мозга, угнетением ресинтеза белков и липидов).
В нервных клетках уменьшается содержание калия и повышается уровень натрия, вследствие чего возникает набухание мозга.
В начале развития симптомокомплекса гипогликемии преобладает активность симпатической НС, при возникновении и углублении коматозного состояния нарастают симптомы ваготонии. При тяжелой и длительной гипогликемии появляются морфологические изменения в виде отека и набухания головного мозга, застойных явлений, рассеянных петехий и кровоизлияний, дегенеративных изменений клеток.
Классификация СД у детей., Классификация СД по ВОЗ (1985)
|
А. Клинические типы |
|
|
Сахарный диабет |
|
|
1. Инсулинзависимый (тип I) |
|
|
2. Инсулиннезависимый (тип II) |
а) у больных с нормальной массой тела б) у больных с ожирением |
|
3. Другие типы СД, связанные с определенными состояниями и синдромами: |
а) заболевания поджелудочной железы б) болезни гормональной природы в) следствие лекарственных и химических повреждений г) повреждения инсулина и его рецепторов д) определенные генетические синдромы е) смешанные причины |
|
Нарушения толерантности к глюкозе |
|
|
У лиц с нормальной массой тела У лиц с ожирением 3. Нарушения ТГ, связанные с другими состояниями и синдромами. |
|
|
Сахарный диабет беременных |
|
|
Б. Статистически достоверные классы риска (нормальная ТГ, но со значительно повышенным риском заболевания): |
|
|
Предшествующие нарушения ТГ Потенциальные нарушения ТГ. |
|
Клиническая классификация СД у детей (В.Г. Баранов, 1981)
|
I. Стадии развития |
1. Предиабет. 2. Скрытый (латентный) диабет. 3. Явный (манифестный) диабет. |
|
II. Степень тяжести |
Легкая (1). 2. Средняя (2). 3. Тяжелая (3) — прекома. 4. Кетонемическая кома. 5. Гиперосмолярная кома. 6. Лактацидемическая кома. |
|
III. Степень компенсации |
1. Компенсация. 2. Субкомпенсация. 3. Декомпенсация. |
|
IV. Течение |
1. Прогрессирующее. 2. Стабильное. 3. Регрессирующее. 4. Лабильное с и без осложнений. |
|
V. Осложнения |
1. Ранние: кетоз, кетоацидоз, кома, жировая инфильтрация печени 2. Поздние: микроангиопатии (нейроретинопатия, гломерулосклероз, поражения сердца и крупных сосудов, синдромы Мориака и Нобекура) |
Пример диагноза: СД, 1 тип (ИЗСД), III степень тяжести, стадия декомпенсации, прогрессирующее течение, осложненный жировой инфильтрацией печени.
Клиническая картина сахарного диабета у детей
сахарный диабет лечение полигенный
Предиабет
Клинически «предиабет» может выставляться:
- Практически здоровому однояйцовому близнецу при наличии СД у второго близнеца.
- Практически здоровому ребенку, оба родителя которого больны СД
- Случай ремиссии после лечения СД
- У взрослых — матерям, родившим мертвого ребенка, у которого в островковом аппарате ПЖ установлена гиперплазия бета-клеток.
Предиабет является клинической формой СД в отличие от «потенциального» диабета или факторов риска его развития, характеризующих повышенную, но не полностью детерминированную, угрозу развития СД.
Факторы риска:
- СД у родственников (один из родителей, братья, сестры).
- Ожирение.
- Масса тела при рождении более 4,1 кг (особенно более 4,5 кг).
- «Сомнительный» тип пробы на ТГ.
- Нарушение обмена липидов.
- Спонтанные гипогликемические состояния у детей от матерей, которые имели в прошлом самопроизвольные выкидыши или внутриутробную смерть плода.
- Врожденные энзимные нарушения обмена углеводов.
Латентный диабет. В этой стадии болезни содержание сахара в крови натощак и в течение суток остается в пределах нормы, в моче сахара нет, но проба на ТГ имеет диабетический тип (классификация ВОЗ эту стадию рассматривает как нарушенная ТГ).
Стандартная проба на ТГ проводится следующим образом: перед проведением пробы обследуемый не менее трех дней должен получать обычное питание без ограничения углеводов, сама проба проводится после 10-16-часового голодания (последний прием пищи не позднее 20.00 вечера).
В течение всего периода исследования ПТГ ребенок находится в покое и в положении сидя или лежа.
Первая проба крови натощак берется после 30-минутного перерыва — физиологического покоя. Далее, в течение 5 минут обследуемый выпивает раствор глюкозы (не менее 10 и не более 50 г, по ВОЗ — не более 75 г) в 200 мл воды с добавлением лимонной кислоты для улучшения вкуса.
Расчет глюкозы для ПТГ: в среднем 1,75 г/кг (50г/м 2 ), по Жуковскому возрастной расчет глюкозы до 1 года 2,5-3 г/кг, в 1-3 года 2 г/кг, старше 3-х лет 1,5-1,75 г/кг.
Далее, в течение 3-х часов каждые 30 минут берут кровь для определения сахара (по упрощенному методу сахар крови определяют через 1 и 2 часа после нагрузки).
По В.Г. Баранову, критерии оценки ПТГ следующие: натощак до 5,5 ммоль/л (до 100 мг%), через 1 час — до 8,9 ммоль/л (до 160 мг%), через 2 часа — до 7,2 ммоль/л (до 130 мг%).
|
Характер пробы |
Натощак |
Через 1 час |
Через 2 час |
|
Здоровый ребенок |
До 5,5 |
До 8,9 |
До 7,2 |
|
Скрытый диабет |
До 5,5 |
Выше 8,9 |
Выше 7,2 |
|
Явный диабет |
Выше 5,5 |
Выше 8,9 |
Выше 7,2 |
|
Сомнительный тип -1 |
До 5,5 |
До 8,9 |
Выше 7,2 |
|
Сомнительный тип-2 |
До 5,5 |
Выше 8,9 |
До 7,2 |
По критериям ВОЗ (1985), показатели гликемии натощак и через 2 часа после нагрузки считаются главными диагностическими цифрами:
|
Характер пробы |
Натощак |
Через 120 минут |
|
Здоровый ребенок |
До 5,6 |
До 7,8 |
|
Нарушение ТГ |
До 6,7 |
7,8 — 11.1 |
|
Явный диабет |
Выше 6,7 |
Выше 11.1 |
Сразу же после проведения ПТГ исследуется моча на сахар — у здорового ребенка глюкозурия отсутствует.
При получении сомнительной сахарной кривой, ПТГ можно повторить через 1-2 недели, причем для выявления менее выраженных нарушений метаболизма за 8,5 и за 2 часа до ПТГ ребенок получает преднизолон (провокация инсулиновой недостаточности) в дозе 6,5 мг/м 2 . Критериями преднизолонглюкозной пробы (ППТГ) являются следующие показатели сахара (в норме): натощак — до 6,7 ммоль/л, через 1 час — до 11,1 ммоль/л, через 2 часа — до 8,4 ммоль/л.
При имеющейся у ребенка клинической картине манифестного СД (глюкозурии, гипергликемии натощак и в течение дня) ПТГ проводить не следует, так как приведенных данных вполне достаточно для диагностики, а проба может утяжелить состояние.
Явный (манифестный) диабет.
В отличие от взрослых ИЗСД у детей прогрессирует быстро: нередко родители замечают появление основной триады симптомов — полируии, полидипсии и похудания — за 1-3 недели до начинающейся диабетической комы, во время которой и диагностируется заболевание. От появления первых симптомов манифестного СД и до развития кетоацидоза у детей школьного возраста проходит обычно 2-4 недели, у детей раннего возраста — от нескольких часов до нескольких дней.
Ранними признаками СД, до развития «больших» симптомов, могут быть, проявляющие себя в течение нескольких месяцев быстрая утомляемость, головокружение, ухудшение сна, недомогание, слабость. Педиатрами часто все эти проявления расцениваются как признаки не диагностируемой вялотекущей инфекции или как невротические состояния. У части детей до появления «больших» симптомов СД отмечаются упорные экземы, фурункулез, ячмени, зуд в области половых органов, кожный зуд. Начальными проявлениями СД у детей могут быть внезапно развивающаяся близорукость или дальнозоркость, боли в ногах, мышечные судороги.
У ряда детей перед выявлением СД отмечено повышенное влечение к сладостям, что связано со спонтанными гипогликемическими состояниями, нередко предшествующими развитию явных проявлений диабета.
Гипогликемия в начальных стадиях СД, видимо, связана с последними попытками ПЖ нормализовать уровень глюкозы в крови, что, в условиях поражения части островков Лангерганса и нарушения гуморальной регуляции, приводит к выбросу в кровь неадекватного количества инсулина (с другой стороны, гиперсекреция инсулина может быть связано с относительной его недостаточностью при предшествующем ожирении).
Помимо повышенной потребности в сладком, могут быть и более выраженные проявления гипогликемии (головные боли, побледнение, потливость, общая слабость, особенно натощак и после физической нагрузки, ночные кошмарные сновидения, возможные обмороки с потерей сознания и гипогликемические судороги).
«Большие» симптомы СД
Полидипсия (жажда), вначале нерезкая, а затем быстро усиливающаяся, связана с высокой гипергликемией и состоянием дегидратации, сопровождается сухостью во рту и жаждой даже в ночное время (несколько раз встают за ночь, чтобы выпить воды).
Жажда носит компенсаторный характер (необходимо восполнить потерю жидкости тканями и организмом в целом), дети выпивают в день от 1,5-2 до 5-6 литров жидкости.
Нередко и у здоровых детей имеется вредная привычка к обильному питью воды (до еды, во время еды), однако ночью не пьют, ночная жажда указывает на возможность СД.
Полиурия при СД является следствием гипергликемии (глюкоза как осмотический диуретик) и призвана уменьшить развитие очень высокой гипергликемии и гиперосмолярности в организме, вывести избыток сахара, кетоновых тел (а с ними — и солей).
Моча светлая или бесцветная, с высокой относительной плотностью за счет выделяющегося сахара, количество ее за сутки 2-6 литров и более.
Родители обычно замечают ночную полиурию (ребенок несколько раз за ночь идет в туалет, опорожняет мочевой пузырь и одновременно пьет, при неаккуратности на полу могут остаться пятна «сахарного сиропа») и, как следствие полиурии с переполнением мочевого пузыря, ночной и дневной энурез.
Похудание отмечается при выраженной глюкозурии из-за дегидратации организма, усиления катаболизма и липолиза при инсулиновой недостаточности. У ряда больных в начальных стадиях отмечается усиление аппетита (полифагия) — свидетельство гиперинсулинизма (до появления «больших» симптомов) и необходимости восполнять содержание белков в связи с усилением их катаболизма и уменьшением массы тела. В последующем, с развитием кетоза, полифагия может смениться снижением аппетита вплоть до анорексии.
Поражения отдельных органов и систем при СД
Кожа и подкожная клетчатка.
- Сухость кожи, выраженная, на ладонях, подошвах, голенях, плечах возникает шелушение, кожный зуд;
- Снижение тургора кожи и подкожной клетчатки (в связи с дегидратацией);
- Быстро развивающиеся потертости могут привести к формированию «диабетической стопы» с омертвением и гангреной конечностей (нельзя разнашивать новую обувь);
- Диабетический рубеоз на щеках, в области надбровных дуг, скул, на подборке, веках (ярко-алого цвета, появляется преимущественно при кетозе, следствие расширения капилляров под воздействием вагуса);
— Ксантоз — пожелтение ладоней и стоп (реже всего тела) в связи с отложением каротина в роговом слое кожи из-за функциональной неполноценности печени с нарушением превращения в ней каротина в витамин А (особенно при избыточном употреблении богатых каротином клюквы, тыквы, моркови, апельсинов, помидоров).
- Ксантомы — плотные узелки желтоватого цвета из наполненных липидами гистиоцитов из-за нарушенного обмена липидов (у детей редки, при терапевтической компенсации диабета могут редуцироваться);
— Липоидный некробиоз — поражения кожи у детей с плохо контролируемыми формами СД на наружной поверхности голеней или в местах введения инсулина, симметричные. Сначала появляется розово-фиолетовый узелок, увеличивается в размере за счет периферического роста, образуется неправильной формы бляшка желтоватого — розовой окраски с множеством телеангиоэктазий на поверхности, бляшка может изъязвляться, после заживления на коже образуется рубцы.
Слизистые оболочки полости рта ярко-красные и сухие. На внутренней поверхности щек десквамация эпителия, напоминающая пятна Филатова-Коплика при кори:
- Язык ярко-красный, лаковый (недостаточность витамин В1)
- Трещины (заеды) углов рта (недостаточность витамина В2)
- Вульвиты и вульвовагиниты у девочек, с зудом в области наружных половых органов.
Мышечная система. Повышенный катаболизм мышечных белков ведет к мышечной слабости и гипотонии, а при тяжелой и длительной декомпенсации возникает атрофия поперечно-полосатой мускулатуры.
Костная система. Иногда отмечается труднообъяснимый локальный остеопороз. Замедление роста отмечено только при длительном декоменсированном диабете (особенно при синдроме Мориака).
Сердце: нечистый I тон на верхушке; систолический шум; приглушение тонов; возможна экстрасистолия; нарушение функциональных сердечных проб с физической нагрузкой; возможно расширение относительной сердечный тупости; признаки гипокалиемии на ЭКГ при кетоациодозе и диабетической коме.
Сосуды: микроангиопатии (нейроретинопатия, интеркапиллярный гломерулосклеороз); нарушение кровообращения нижних конечностей (у детей редко).
Поражение глаз . Диабетическая нейроретинопатия — дегенеративные изменения нервных и сосудистых элементов сетчатки, приводящие к снижению остроты зрения и слепоте. Развитие нейроретинопатии определяется не столько со сроком, сколько тяжестью СД. Диабетическая катаракта (помутнение хрусталика, связанное с длительной декомпенсацией обменных процессов из-за отсутствия или неправильного лечения), может появляться в ранние сроки заболевания (через 2-3 года после выявления СД), иногда замечается одновременно с выявлением заболевания.
Поражение почек. При впервые выявленном СД отмечается повышение фильтрационной способности почек и снижение уровня фильтрации до нормального на фоне лечения инсулином (связано с метаболическими нарушениями).
При выраженной декомпенсации СД во время диабетической прекомы и комы в моче может появиться протеинурия и форменные элементы по типу ОПН (гематоренальный синдром Альтгаузена-Соркина).
Одним из самых тяжелых осложнений СД, приводящим к развитию ХПН вплоть до уремии, является диабетический капиллярный гломерулосклероз (синдром Киммельстилла-Уилсона).
Обычно наличие диабетической нейроретинпатии повышает опасность гломерулосклероза. Ранним проявлением гломерусклероза служит постоянная или периодическая протеинурия. При прогрессировании гломерулосклероза увеличивается альбуминурия, нарастает гиперхолестеринемия, гипопротеинемия, гиперазотемия, повышается артериальное давление, появляются отеки и возможно развитие уремии. В терминальной фазе может наступить резкое понижение потребности в инсулине с нормогликемией и аглюкозурией.
Нервная система. Причинами поражения ЦНС являются тяжелые обменные нарушения при декомпенсации СД и лабильное его течение с частыми гипогликемиями. Нарушения функции ЦНС носит характер неврозоподобных состояний (диабетическая энцефалопатия) с преимущественным поражением эмоциональной сферы, пирамидной и мозжечковой системы: жалобы на головную боль, головокружение; родители замечают повышенную раздражительность, плаксивость, негативизм к инъекциям; выявляются вазомоторная лабильность, потливость, акроцианоз (признаки невроза).
Внутренняя картина болезни при СД представляет сложную динамично структурированную систему, зависящую от возраста, пола, длительности и тяжести заболеваниям, что требует выделения групп нервно-психического риска.
Поражение периферической НС проявляется в виде неврита и невралгии черепно-мозговых нервов, полиневрита, радикулита и полирадикулита. Чаще встречаются проявления полиневрита (жалуются на боли в конечностях по ходу нервных стволов, наблюдается парестезии и судороги); объективно определяются гипо- или гиперальгезия, нарушения тактильной и (реже) глубокой чувствительности, возможны изменения корешкового и смешанного типа; у отдельных больных снижаются или отсутствуют рефлексы.
Желудочно-кишечный тракт. Повышение секреции амилазы слюнными железами сопровождается хроническим неспецифическим увеличением околоушных желез, постоянно или периодически (при этом болезненности при пальпации и жевании нет, гипертермии нет).
Парадонтоз у детей с СД встречается чаще, чем у здоровых (особенно при тяжелом и длительно текущем диабете).
Гастродуоденит развивается вместе с диабетическими проявлениями (ацидоз, кетонемия, нарушение электролитов, далее — микроангиопатии).
В начальном периоде гастродуоденит представлен преимущественно поверхностной воспалительной инфильтрацией, а при более тяжелом течении помимо более выраженной инфильтрации имеются признаки атрофии.
Печень. Гепатомегалия при декомпенсированном СД связана с усиленным отложением в ней жира (при правильном лечении размеры печени уменьшаются, но при длительно существующей жировой инфильтрации в печени могут развиться цирротические изменения).
Гепатомегалия сопровождается рядом функциональных печеночных нарушений — диспротеинемией (снижение синтеза белка), гиперхолестеринемией, периодическими нарастанием непрямого билирубина (из-за холестаза).
Как обязательный симптом, гепатомегалия входит в структуру следующих поздних осложнений:
- Синдром Мориака — значительная задержка роста с избыточным отложением жира на груди, животе и бедрах, округлым лунообразным лицом с яркими щеками: в пубертатном периоде выявляется задержка полового развития;
- у всех детей значительно увеличена печень без сопутствующего увеличения селезенки или асцита;
- одинаково часто поражаются мальчики и девчонки, дети с этим осложнением, как правило, заболевают СД в раннем возрасте и имеют в течение нескольких лет тяжелое течение заболевания.
- Синдром Нобекура наблюдается реже, характеризуется жировой инфильтрацией печени с ее увеличением, отставанием роста и полового развития у детей с пониженной массой тела.
Диагностика СД
Для диагностики СД большое значение имеют:
- Определение уровня сахара в крови натощак и в течение суток (гликемический профиль);
- Динамика уровня сахара при различных типах ПТГ;
- Определение уровня сахара в моче и колебания его в течение суток (глюкозурический профиль);
- Определение содержания кетоновых тел в крови и моче;
- Определение показателей КОС крови.
Сахар крови
Для экспресс — диагностики используются одноразовое иглы для забора крови из мякоти пальца и диагностические полоски бумаги, на которые наносится капля крови — по изменению цвета индикаторной полоски при сопоставлении с цветовой шкалой можно судить о концентрации сахара в крови.
Разработаны электронные глюкометры.
В стадиях предиабета и латентного диабета проводится описанная выше проба на ТГ (или преднизолонглюкозная проба).
В стадии явного диабета при поступлении в стационар определяется гликемический профиль — показатели сахара крови каждые 3-4 часа в течение суток на фоне проводимого лечения, питания и режима для коррекции проводимой инсулинотерапии.
Сахар мочи
Глюкозурия
глюкозурического профиля —
Кетоновые тела, Кетоновые тела, Кислотно-основное состояние, Лечение СД у детей
Основная цель лечения детей с ИЗСД — максимальная компенсация нарушенного обмена веществ. По В.Л. Лисс, критериями компенсации являются стойкая нормогликемия, аглюкозурия и уровень гликолизированного гемоглобина не выше 7-9%.
Уровень гликолизированного Нв (Нв, к которому без участия ферментов присоединена молекула глюкозы) зависит от длительности и степени гипергликемии: повышение его уровня выше 7% свидетельствует о повышении среднего уровня гликемии за предшествующие 2-3 месяца.
В педиатрической практике используется принцип компенсации, предложенный М.А. Жуковским (с учетом риска развития гипогликемической комы на фоне инсулинтерапии):
- Гипергликемия в пределах 11,0 ммоль/л.
- Глюкозурия в пределах 5% сахарной ценности пищи (выраженная в граммах сумма углеводов и половины белков, имеющихся в суточном рационе питания).
Основными задачами лечения СД по рекомендациям экспертов ВОЗ, дополненных А. Древалем (1993), являются:
- Нормализация обмена веществ — углеводов (нормогликемия, аглюкозурия, норма гликолизированного Нв) и липидов (нормолипидемия);
- Нормализация нутритивного статуса;
- Достижение и поддержание нормальной массы тела;
- Обеспечение нормального роста и развития детей;
- Устранение клинической симптоматики (общая слабость, жажда, полиурия) и предотвращение острых метаболических нарушений (гипогликемия, кетоз, кетоацидоз);
- Предотвращение или задержка развития поздних осложнений СД (микро- и макроангиопатий, нейроретинопатии, гломерулосклероза), их адекватное лечение;
- Профилактика интеркуррентных инфекций.
Режим дня и ухода
В состоянии компенсации ребенок находится на общем режиме, посещает школу, получает умеренные физические нагрузки (улучшают утилизацию глюкозы).
Физические нагрузки при СД должны быть умеренными (утренняя гимнастика, физкультура без перегрузок), дозированными (четкое распределение по времени суток — по часам посталиментарной гипергликемии и интенсивности), с положительной эмоциональной окраской.
При начинающейся декомпенсации ребенок полностью освобождается от физических нагрузок, в прекоматозном состоянии — переводится на постельный режим. В связи с частыми микробными и дрожжевыми поражениями кожи и слизистых (вульвовагиниты у девочек) необходим тщательный санитарно-гигиенический уход (гигиена кожи, полости рта, наружных половых органов).
Необходимость проведения профилактических прививок детям с СД практическими эндокринологами категорически отрицается (в связи с провоцированием антигенного поражения поджелудочной железы).
Диета
Диетотерапия является одним из определяющих элементов концепции лечения СД, направленного на нормализацию обменных нарушений. Несоблюдение диеты немедленно приводит к декомпенсации и неоправданному дополнительному введению инсулина.
Общие принципы диетотерапии (А. Древаль) включают ограничение продуктов с высоким содержанием простых углеводов (глюкозы, сахарозы), относительно равномерное распределение приема углеводов в течение дня, соответствие калорийности диеты энергозатратам больного. По Э.П. Касаткиной (1986) энергетическая ценность и состав суточного рациона должны соответствовать физиологическим потребностям организма, полностью исключены рафинированные углеводы. Время приема пищи и дозирование углеводов в течение суток должны четко соблюдаться. Должны быть ежедневный контроль питания, подсчет сахарной ценности каждого приема пищи.
По М.А. Жуковскому, калорийность пищи и ее состав при СД у детей должны приближаться к нормам питания здоровых, но при определении калорийности должны учитываться возраст (периоды интенсивного роста) и образ жизни (интенсивная физическая нагрузка или гиподинамия), а также дефицит или избыток массы тела.
В случаях впервые выявленного СД или при выраженной его декоменсации в зависимости от степени тяжести уменьшают количество легкоусвояемых углеводов при одновременном увеличении белков (до верхних границ норм), на фоне, которого подбирается инсулинотерапия. При компенсации СД соотношение белков, жиров и углеводов выравнивается по возрастным нормам. Режим питания больного ИЗСД состоит, как минимум, из 4-х приемов пищи: завтрак, обед, ужин и прием пищи на ночь. Наиболее рациональный режим включает еще два дополнительных приема пищи: между завтраком и обедом (2-й завтрак) и обедом и ужином (полдник).
Суточный калораж рассчитывается по таблицам питания для больных СД, либо по ориентировочным формулам. По Н.И. Дедову (1990) суточный калораж пищи для больных СД при нормальном росте и МТ по возрасту должна соответствовать таковым у здоровых детей.
Формула расчета суточной калорийности пищи (по Н.И. Дедову):
Суточный калораж =1000+(100х число лет)
где, 1000 — суточный калораж годовалого ребенка (ккал).
Например: подросток 14 лет, суточный калораж = 1000+(100 х 14) = 1000+1400 = 2400 ккал.
Суточная калорийность пищи в течение дня должна распределяться так:
|
1. Завтрак в 9.00 |
25% (600 ккал из 2400) |
|
2. 2-й завтрак в 12.00 |
20-15% (240-360) |
|
3. Обед в 14.00 |
25-30% (600-720) |
|
4. Полдник в 17.00 |
20-25% (600-720) |
|
5. Ужин в 19.00 |
20-25% (600-720) |
|
6. 2-й ужин в 23.00 |
5-10% (120-240) |
Соотношение БЖУ в суточном калораже должно соответствовать 40-50% углеводов, 20-25% жиров и 30% белков, что близко к таковому у здоровых детей.
Сгорая, 1 г углеводов или белков выделяет 4 ккал энергии, а 1 г жира — 9 ккал. Отсюда, можно рассчитать суточное количество необходимых ребенку основных пищевых ингредиентов.
Н-р, для подростка 14 лет при суточной калорийности 2400 ккал необходимо:
- углеводов = (50% от 2400) : 4= 1200 : 4 = 300 г
- белков = (30% от 2400) : 4 = 720 : 4 = 180 г
- жиров = (20% от 2400) : 9 = 480 : 9 = 53 г
Углеводы обеспечивают до 50% суточной калорийности (8-12 г/кг/сутки).
Прием легкоусвояемых углеводов при латентном СД вызывает гипергликемию с выбросом последних запасов инсулина и истощением бета-клеток, повышает резистетность тканей к инсулину; при манифестном СД они вызывает резкую и быструю гипергликемию, требующую больших доз экзогенного инсулина. К легкоусвояемым углеводам относятся сахар, мед, конфеты, шоколад, пшеничная мука и изделия из нее (вермишель, макароны), манная рисовая крупа, фрукты с большим содержанием глюкозы (виноград, бананы, хурма, финики, сладкие груши и вишни), сладкие вина, соки, сиропы, сладкие газированные напитки.
Необходимое для питания количество углеводов ребенок получает с продуктами богатым клетчаткой, замедляющей всасывание углеводов -ржаная мука, пшеничная мука с добавлением отрубей (остатки оболочки зерна, получаемые после размола), крупы (гречневая, пшенная, перловая, овсяная), картофель.
Стандартные порции продуктов, Таблица эквивалентной замены продуктов по углеводам в граммах
|
Продукты |
Эквивалент хлебной ценности (в гр.) |
|
Ржаной хлеб Крупы гречневая, пшеничная, овсяная, перловая Каша рисовая Картофель Пшеничный хлеб с 10% отрубей Макаронные изделия Морковь Свекла Зеленый горошек Яблоки, крыжовник Клубника, смородина, земляника Апельсины, персики, груши, дыни, сливы Абрикосы, брусника, черника, малина Арбузы, вишня, черешня, мандарины Молоко |
25 20 15 60 25 15 175 120 170 100 150 80 130 50 250 |
Для удобства пользования разработаны и более простые таблицы эквивалентной замены продуктов по углеводам. 1 хлебная единица содержится в следующих количествах пищевых продуктов: 1 стаканы молока (250 мл), 2 столовых ложки риса, вермишели, макарон, 1 кусок ржаного хлеба (30 г), 1/2 початка кукурузы, 1 груша, 1/2 грейпфрута, 15 вишен (110 г), 1 персик (140 г), 1/2 стакана апельсинового сока (100 мл), 1 стакан кефира (250 мл ), 1/2 булочки (25 г), 1 кусок белого хлеба (30 г), 1 картофелина (80 г), 1 яблоко (100 г),1 апельсин (130 г), 1/2 банана (60 г), 10 клубничин, 1 блюдце сметаны (120 г), 1 кусок дыни, 5 крекеров (40 г).
При замене продуктов с помощью таких таблиц допускается, что все они дают один и тот же гипергликемический эффект, однако при приеме содержащих одно и то же количество углеводов 100 г картофеля и винограда посталиментарная гипергликемия в последнем случае оказывается выше.
Гликемический индекс (Дженкинса)
Фиксированное во времени распределение углеводов в течение суток. При введении пролонгированного инсулина больной должен получать углеводы через 1 час после инъекции и далее каждые 2-3 часа в течение максимального действия препарата (12 часов).
При введении короткодействующего инсулина — через 20-30 минут после введения. Если больной находится на «физиологическом» режиме введения инсулина (самостоятельно меняет дозу), то он может самостоятельно менять и питание исходя из того, что на 1 хлебную единицу (12 г углеводов) вводится 1,3 ЕД инсулина и 1 хлебная единица повышает уровень глюкозы крови на 2,8 ммоль/л.
Из питания больного СД исключаются сахар и сахаросодержащие продукты . Набор углеводистых продуктов в таблицах замены включает сахарозу содержащих продуктов для нерегулярного (эпизодического) приема (мороженное, кондитерские изделия).
Для приготовления бессахарных диабетических продуктов широко используются заменители сахара (ксилит, сорбит, маннит) калорийность у которых равна таковой у сахарозы (4 ккал/кг).
Фруктоза , по американским данным, лишь немногим слаще сахара, но после ее приема гликемия возрастает значительно меньше, чем после других углеводов.
Стевиозид — сахарозаменитель, получаемый из листьев стевии или непосредственно измельченный лист стевии. Из искусственных сахарозаменителей чаще используются аспартам и сахарин. Аспартам (сладекс) — химическая комбинация двух (несладких на вкус по отдельности) аминокислот (L-фенилаланина и L-аспарагина).
Эта химическая комбинация в 200 раз слаще сахарозы (как подсластителя ее требуется в 200 раз меньше), а потому практически не влияет на калорийность продуктов. Аспартам нестабилен при высоких температурах и применение его в кулинарии ограничено. Сахарин в 300 раз слаще сахарозы, но имеется предрасположенность к развитию рака мочевого пузыря.
Жиры обеспечивают 20-25% суточной калорийности (1,5-4 г/кг/сутки).
При их назначении в питании учитываются склонность к ожирению, кетозу и непереносимости жира, а также высокий риск развития атеросклероза у больных диабетом. Любая диета при СД должна иметь гиполипидемическую направленность. Полностью исключаются продукты, содержащие тугоплавкие жиры (источники насыщенных жирных кислот) из-за опасности жировой инфильтрации печени и повышенного образования кетоновых тел (говяжье и свиное сало, гусиный и бараний жир).
Сливочное масло применяют в минимальных количествах, необходимых для кулинарной обработки продуктов. При кетоацидозе жиры из питания полностью исключаются. В качестве жиров в питании применяют продукты, содержащие ННЖК, снижающие уровень триглицеридов и холестерина в крови (растительные масла -подсолнечное, кукурузное), которые должны составлять 1/3 жиров пищи.
Для нормализации жирового обмена (удаление жиров из печени путем образования фосфолипидов) используются молодая баранина и свинина нежирных сортов, телятина, молоко, овсяная крупа, творог, треска.
Белки составляют 30% суточного калоража (2-3,5 г/кг/сутки, в период интенсивного роста 3-4 г/кг/сутки).
Белков животного происхождения, с более высоким содержанием незаменимых аминокислот, должно быть не менее половины (молоко, творог, нежирное мясо, рыба, яйца).
Значительное обеднение пищи белками приводит к задержке роста, анемии, снижает сопротивляемость организма. В осенне-зимний период необходимо обратить внимание на достаточную витаминизацию пищи.
Пероральные антидиабетические препараты (ПАДП)., Инсулинотерапия
Все дети с манифестной формой СД подлежит лечению инсулином. Препараты инсулина различаются по происхождению и продолжительности действия. Инсулин животного происхождения (получают из ПЖ крупного рогатого скота или свиней) в педиатрической практике практически не используются.
Синтетические инсулины (новоинсулины)
Преимущества синтетического (рекомбинантного) инсулина:
- меньший риск иммунологических реакций (идентичен человеческому);
- апирогенность;
- не загрязнен другими пептидными гормонами.
В зависимости от продолжительности действия, инсулины делятся на три группы:
1. Быстродействующие инсулины: начало действия через 30 минут после введения, максимум эффекта между 2-3 (2,5-5) часами, продолжительность — до 6 (8) часов. Форма выпуска — флаконы для шприца-ручки (пенфиллы) по 1-1,5 мл (1 мл = 100 ЕД).
Коммерческие формы: Актрапид НМ и МС (Ново-Нордиск, Дания); Хумулин Р (Эли Лилли, США); Иллентин-II-регулятор, Хумулин-регулятор (Элли Лилли, США); Инсуман-нормаль (Хехст, ФРГ); Берлинсулин Н-нормаль (Берлин-Хеми, ФРГ).
Лучший препарат хумалог (Эли Лилли, США), действие начинается через 10-15 минут после введения и продолжается 3-4 часа.
2.Инсулины средней продолжительности действия:
3.Инсулины длительного действия:
Помимо вышеперечисленных препаратов выпускаются двухпиковые (смешанные) инсулины комбинированного действия — комбинации инсулинов короткого действия и средней продолжительности действия. Создание таких инсулинов преследует цели создания стойкой компенсации диабета, с одной стороны, и уменьшения количества инъекций, с другой.
Фирма Эли Лилли (США):
- «Профиль» №1 — 10% инсулина короткого действия (регулярно или нормально) + 90% инсулина средней продолжительности действия (НПХ или изолипана);
- «Профиль» №2 — 20 + 80% соответственно;
- «Профиль» №3 — 30 + 70% соответственно;
- «Профиль» №4 — 40 + 60% соответственно;
Фирма Берлин-Хеми:
1. пенфиллы «Берлининсулин-Н-10/90» (10 и 90% соответственно);
2. пенфиллы «Берлининсулин-Н-20/80» (20 и 80% соответственно);;
3. пенфиллы «Берлининсулин-Н-30/70» (30 и 70% соответственно);;
4. пенфиллы «Берлининсулин-Н-40/60» (40 и 60% соответственно);;
Фирма Ново-Нордиск:
1. пенфиллы «Микстард 10 НМ» (10% короткого + 90% средней продолжительности);
2. пенфиллы «Микстард 20 НМ» (20% короткого + 80% средней продолжительности);;
3. пенфиллы «Микстард 30 НМ» (Актрафан НМ = 30% короткого + 70% протофана);
4. пенфиллы «Микстард 40 НМ» (40% короткого + 60% средней продолжительности);;
5. пенфиллы «Микстард 50 НМ» (50% короткого + 50% средней продолжительности);;
Фирма Хехст:
- инсуман комб-Н-инсулин (50% инсулина короткого действия + 50% инсулина базаль);
- инсуман депо-Н-инсулин (25+75% соответственно);
- инсуман депо-15-инсулин (15 и 85% соответственно).
Перед инъекцией все эти препараты тщательно перемешиваются!
Типы инсулинов и продолжительность их действия (Б.С.Ольсен, Х.Мортенсен, 2001)
|
Препарат |
Начало действия |
Пик действия |
Максимальная длительность |
|||
|
Короткого действия (актрапид) |
0,5-1 час |
1-3 часа |
6-8 часов |
|||
|
Средней продолжительности (протофан) |
1.5-2 часа |
4-12 часов |
18-24 часа |
|||
|
Готовая смесь 10*/90** (микстрад 10) |
5-10 часов |
18-24 часа |
0,5-1 час |
5-10 часов |
18-24 часа |
|
|
Готовая смесь 30*/70**(микстрад 30) |
0,5-1 час |
5-9 часов |
18-24 часа |
|||
|
Готовая смесь 40*/60**(микстрад 40) |
0,5-1 час |
1-3 часа |
18-24 часа |
|||
|
Готовая смесь 50*/50**(микстрад 50) |
0,5-1 час |
1-3 часа |
18-24 часа |
|||
|
Быстродействующий аналог инсулина (аспарт) |
10-20 минут |
1-3 часа |
3-5 часов |
* растворимый инсулин (короткодействующий)
** изофанинсулин (средней продолжительности)
Инсулины во флаконах для шприц-ручек хранят при температура +2 +8 ºС, нельзя замораживать! Флакон, находящийся в применении, а также запасной флакон могут храниться при комнатной температуре (до +25ºС) в темном месте не более 1 месяца. Срок годности 24 месяца.
Для введения инсулинов используется шприц-ручка (ручной полуавтоматический дозатор для подкожного введения).
Различают шприц — ручки для введения инсулина короткого и быстрого действия (Пливален -1, Югославия; Новопен-1, Дания; Оптипен-1, Хехст; Белинпен-1, Берлин-Хеми; Лиллипен, Эли Лилли; Инсулпен-1, Россия), при каждом нажатии ручки на корпусе выделяется 2 ЕД инсулина и шприц-ручки для введения инсулина как короткого, так и длительного действия (Пливален-2, Новопен-2, Оптипен-2, Берлинпен-2, Инсулпен-2), одномоментно можно ввести от 2 до 36 ЕД инсулина.
Инсулин, используемый в шприц-ручках, выпускается в специальных флаконах — пенфиллах (картриджах или баллончиках), которые содержат 1, 1,5 или 3 мл инсулина в концентрации 100 ЕД. в 1 мл.
Инъекции инсулина короткого действия рекомендуется делать в подкожную клетчатку живота, вводя иглу под углом 45° (у худых пациентов во избежание попадания инсулина в мышцу необходимо использовать иглы длиной 8 мм).
Инъекции инсулина средней продолжительности действия или готовых смесей инсулина рекомендуется делать в подкожную клетчатку передней части бедер или ягодиц, вводя иглу под углом 45°. Не рекомендуется протирать места инъекций спиртом. Места инъекция необходимо менять. Нельзя делать инъекции в места с инфильтрацией или липодистрофией, из которых всасывание инсулина непредсказуемо.
При поступлении в клинику лечение манифестного СД без признаков кетоацидоза начинают с инсулинов короткого действия (актрапид) в дозе 0,5 ЕД/кг/сут. Инсулин короткого действия вводят подкожно 4-5 раз в сутки за полчаса до еды: перед завтраком 50% дозы, перед обедом 15-20%, перед ужином 20-25%, перед сном 5-10%.
С учетом более высокой, чем у взрослых, чувствительности ткани ребенка к инсулину, вначале вводится не вся разовая доза, а 2/3 или 1/2. В первый же день проводится контроль гликемического и глюкозурического профиля для оценки действия назначенной дозы инсулина и ее коррекции с учетом суточной глюкозурии.
Пример: Ребенок 6 лет, манифестный СД. Глюкозурический профиль после первоначальной дозы инсулина в день госпитализации определился следующим образом:
|
1. |
9-14 часов |
300 мл |
150 г/л сахара |
|
2. |
14-19 часов |
350 мл |
135 г/л сахара |
|
3. |
19-23 часа |
120 мл |
250 г/л сахара |
|
4. |
23- 6 часов |
300 мл |
80 г/л сахара |
|
5. |
6-9 часов |
200 мл |
50 г/л сахара |
Расчет инсулина начинается с определения фактической глюкозурии в каждой порции мочи:
- 150 г содержится в 1000 мл, Х г — в 300 мл; Х = (300 х 150) : 1000 = 45 г.
135 г содержится в 1000 мл, Х г — в 350 мл; Х = (350 х 135) : 1000 = 47 г.
120 г содержится в 1000 мл, Х г — в 250 мл; Х = (250 х 120) : 1000 = 30 г.
80 г содержится в 1000 мл, Х г — в 300 мл; Х = (80 x 300) : 2000 = 24 г.
50 г содержится в 1000 мл, Х г — в 200 мл; Х = (50 х 200) : 1000 = 10 г.
Суточная глюкозурия = 45 + 47 + 30 + 24 + 10 = 156 г.
Расчет инсулина исходит из того, что 1 ед. инсулина утилизирует 5 г глюкозы. По В.Г. Баранову, расчет проводится до полной аглюкозурии. У приведенного больного равняется (156 : 5 = 31) 31 единица инсулина в сутки.
Однако при расчете до полной аглюкозурии возможна передозировка инсулина с последующим развитием гипогликемической комы. Поэтому, по М.Г.Жуковскому, на определенную часть глюкозы инсулин предлагается не рассчитывать (так называемые 5% от сахарной ценности пищи).
Сахарная ценность пищи = сумма 100% суточной потребности детей в углеводах и 50% суточной потребности в белках в граммах. Определение суточной потребности в белках и углеводах ведется по соответствующим таблицам.
Суточная потребность детей, больных сахарным диабетом, в углеводах и белках в граммах (М.А.Жуковский)
|
Возраст |
Углеводы |
Белки |
|
1-1,5 года |
156 |
53 |
|
1,5-3 года |
174 |
58 |
|
3-5 лет |
213 |
71 |
|
5-7 лет |
238 |
79 |
|
7-11 лет |
276 |
92 |
|
11-15 лет |
323 |
108 |
В примере, для ребенка 6 лет в суточном рационе содержание углеводов достигает 238 г, белков — 80 г. Отсюда сахарная ценность пищи = 238 + (80 : 2) = 238 + 40=278 г. 5% сахарной ценности пищи в данном случае = 278 х 0,05 = 14 г.
г — количество сахара, которое может выделиться с мочой, а всю остальную глюкозурию необходимо утилизировать инсулином.
- 14 = 142 г сахара
: 5 = 28 единиц инсулина в сутки.
Учитывая высокую чувствительность тканей ребенка к экзогенному инсулину, первоначально назначается 2/3 дозы, в нашем примере 20 единиц в 4 введения:
8.30 — 8 ед. 2) 13.30 — 6 ед. 3) 18.30 — 4 ед. 4) 24.00 — 2 ед.
В дальнейшем общая доза инсулина и распределение ее будет зависеть от показателей контрольных гликемических и глюкозурических профилей. По мере стабилизации состояния, введение инсулинов короткого действия комбинируется с введением инсулинов длительного действия и на этой схеме ребенок переводится на амбулаторное наблюдение.
Суточная потребность в инсулине изменяется с течением времени и стадией полового развития:
- Во время фазы ремиссии суточная доза инсулина обычно менее 0,5 ед/кг в сутки.
- Во время препубертата суточная доза инсулина составляет 0,6-1,0 ед/кг в сутки.
- Во время пубертата суточная доза инсулина составляет 1,0-2,0 ед/кг в сутки.
- После пубертатного скачка в росте потребность в инсулине обычно снижается и соответствует потребности в период препубертата.
Режим инсулинотерапии подбирается индивидуально. Предпочтение отдается наиболее простому режиму, обеспечивающему приемлемый метаболический контроль. Введение более свободного режима дня с течением времени влечет за собой необходимость соответствующих изменений в режиме инсулинотерапии. Наиболее широко используются следующие режимы инсулинотерапии:
- Две инъекции инсулина в день: перед завтраком и перед ужином — сочетание инсулинов короткого действия и средней продолжительности.
При этом 2/3 суточной дозы инсулина вводится перед завтраком и 1/3 — перед ужином. Кроме этого, 1/3 каждой инъекции должен составлять инсулин короткого действия и 2/3 — инсулин средней продолжительности.
- Три инъекции инсулина в день: комбинация инсулинов короткого действия и средней продолжительности перед завтраком, инъекция инсулина короткого действия перед ужином и инъекция инсулина средней продолжительности перед сном.
При этом 40-50% суточной дозы инсулина вводится перед завтраком: 2/3 составляет инсулин средней продолжительности и 1/3 — короткого действия. 10-15% суточной дозы приходится на инъекцию короткодействующего инсулина перед ужином, и 40% суточной дозы приходится на инъекцию инсулина средней продолжительности действия перед сном.
- Базис-болюсная терапия (терапия многократными инъекциями) — инъекции инсулина короткого действия перед основными приемами пищи и инъекция инсулина средней продолжительности действия перед сном.
При этом 30-40% суточной дозы приходится на инсулин средней продолжительности действия, который вводится перед сном. Остальная суточная доза распределяется в виде инъекций инсулина короткого действия перед основными приемами пищи в соответствии с показателями сахара крови и планируемой едой. По рекомендациям М.И. Балаболкина и соавт., можно использовать следующие схемы комбинации инсулинов короткого и длительного действия:
Первая схема
Традиционная терапия с двумя инъекциями короткого и пролонгированного инсулинов (Актрапид, Протофан) перед завтраком и перед ужином. При этом обеспечивается достаточное насыщение организма инсулином в течение суток, имеется возможность своевременной коррекции утренней и вечерней дозы при изменении режима дня, питания и нагрузок.
Утренняя инъекция должна составлять 2/3 от суточной дозы, вечерняя — 1/3. Соотношение Протофан/Актрапид в утренней и вечерней инъекциях должно быть 2:1. Если общая доза инсулина составляет 36 ед. в сутки, то 24 ед. будет приходиться на утреннюю инъекцию и 12 — на вечернюю. При этом утром ребенок будет получать 16 ед. Протофана и 8 ед. Актрапида, а вечером 8 ед. Протофана и 4 ед. Актрапида.
Коррекция дозы
— При жажде, выделении большого количества мочи и гипергликемии между завтраком и обедом дозу Актрапида на следующее утро перед завтраком увеличивают на 2-4 ед. (одномоментное изменение дозы не должно превышать 10% от ее первоначальной величины, что в практике как раз соответствует 2-4 ед.).
- Если несколько дней подряд имеются повышенная жажда, избыточное мочеотделение и гипергликемия между обедом и ужином, утреннюю дозу Протофана увеличивают на 2-4 ед.
- Если эти симптомы появляются в промежутке между ужином и сном, а в первую половину ночи приходится вставать мочиться, дозу инсулина Актрапид перед ужином увеличивают на 2-4 ед.
- Если во второй половине ночи больной несколько раз встает мочиться, а натощак утром имеется жажда, гипергликемия и повышенная глюкозурия в утренней моче, перед ужином увеличивают Протофан на 2-4 ед.
— При необъяснимой гипогликемии между завтраком и обедом дозу инсулина Актрапид на следующее утро уменьшают на 2-4 ед. То же самой необходимо сделать, если предполагаемый завтрак будет меньше, чем обычно, или в промежутке между завтраком и обедом планируется интенсивная физическая нагрузка.
- Если отмечается гипогликемия между обедом и ужином в течение 2-3 дней подряд, дозу Протофана перед завтраком уменьшают на 2-3 ед., то же самое проводится, если предстоит интенсивная физическая нагрузка.
- Если в течение 2-3 дней подряд имеется гипогликемия после ужина, дозу Актрапида перед ужином уменьшают на 2-4 ед., то же самое проводят, если предстоит интенсивная физическая нагрузка после ужина.
— Если наблюдается гипогликемия в течение ночи (потливость, ощущение разбитости, головные боли после сна, кошмарные сновидения, повторяющиеся в течение нескольких ночей), перед ужином уменьшают дозу Протофана на 2-4 ед.
Вторая схема
Интенсифицированная терапия с одной базальной инъекцией пролонгированного инсулина (Протофан) перед сном (в 22-23 часа) и «подколками» короткого действия инсулина (Актрапид) перед каждым приемом пищи.
Из суммарной суточной дозы 30-40% вводится перед завтраком и обедом и 20-30% перед ужином в виде «подколок» Актрапида в дозе, зависящей от вида и количества углеводов в пище.
Если суточная доза инсулина составляет 36 ед., то 16 ед. будет приходиться на вечернюю инъекцию Протофана, а перед каждым приемом пищи (завтрак, обед, ужин) подкалывается Актрапид по 6-8-6 ед. соответственно.
Коррекция дозы
- Если в течение 2-3 ночей подряд больной несколько раз встает мочиться, а натощак имеется жажда, гипергликемия и повышение содержания глюкозы в утренней моче, то дозу Протофана увеличивают на 2-4 ед.
- Если жажде, полиурия и гипергликемия отмечаются после приема пищи, то необходимо увеличить «подколку» Актрапида на 2-4 ед.
перед тем приемом пищи, после которого отмечаются эти явления.
- Если в течение 2-3 ночей подряд отмечается гипогликемия, то дозу Протофана вечером уменьшают на 2-4 ед.
- Если после приема пищи была гипогликемия, то дозу Актрапида перед соответствующим приемом пищи уменьшают на 2-4 ед. Аналогично поступают, если после еды предстоит интенсивная физическая нагрузка.
При второй схеме в большей степени имитируется физиологическое поступление инсулина, упрощаются и делаются более удобными инъекции.
На практике используется комбинация из вышеприведенных схем, когда присутствуют утренняя и вечерняя инъекции пролонгированного инсулина, и подколки быстродействующего инсулина перед каждым приемом пищи.
Инсулиновые правила
1. Появление больших симптомов СД (жажда, полиурия, похудание) всегда требует госпитализации и назначения препаратов инсулина.
- Лечение начинают с инсулинов короткого действия, расчет первичной дозы при впервые выявленном СД без кетоза 0,5 ед/кг в сутки. Детям раннего возраста доза уменьшается до 0,12-0,25 ед/кг.
- Подбор суточной дозы инсулина в последующие дни осуществляется по показателям гликемического и глюкозурического профиля.
- Отсутствие кетоза и стабилизация состояния служит показанием для подключения инсулинов длительного действия и перехода на комбинированные схемы инсулинотерапии.
Осложнения инсулинотерапии
1. Хроническая недостаточность эндогенного инсулина с сохранением умеренной гипергликемии вызывает задержку роста, полового развития, гепатомегалию, ранние сосудистые осложнения (синдром Мориака).
— Хроническая передозировка инсулина (синдром Сомоджи) характеризуется повышенным аппетитом, ускорением роста, ожирением (по кушингоидному типу), гепатомегалией, склонностью к ацидозу и кетозу, гипогликемическими состояния (преимущественно ночью и утром), гипергликемией, ранней микроангиопатией.
— Гипогликемия (снижение сахара крови ниже 3,0 ммоль/л) развивается при избыточном введении инсулина, сниженном поступлении или повышенном расходе глюкозы (нарушение диеты, физическая нагрузка).
Первые симптомы обусловлены активацией симпатико-адреналовой системы (тремор, тахикардия, потливость, слабость, диплопия, повышенный аппетит, боли в животе), затем появляются признаки поражения ЦНС (немотивированный плач, агрессивность, возбуждение сменяется сонливостью, афазия — нарушение речи, парезы, локальные или общие клонико-тонические судороги, потеря сознания по типу гипогликемической комы).
Повторные гипогликемии требуют неврологического обследования для дифференциальной диагностики с эпилепсией.
4. «Инсулиновые отеки» возникают при передозировке инсулина, особенно при избыточной инфузионной терапии в ходе лечения диабетической комы. Особенно опасен отек мозга, появляющийся через несколько часов от начала лечения (обусловлен быстрым снижением уровня внеклеточной глюкозы при сохранением повышенной концентрации глюкозы в клетке, что ведет к гипергидратации клеток мозга).
Клинически отек мозга проявляется ухудшением состояния, появлением неврологической симптоматики, углублением комы у ребенка на фоне интенсивной терапии диабетической комы. Отеки могут также развиться в легких, ПЖК, внутренних органах. Быстрая, в течение нескольких часов, прибавка массы у больного СД требует немедленного снижения дозы инсулина и коррекции инфузионной терапии.
— Липодистрофии появляются в местах инъекций инсулина животного происхождения. Для их профилактики рекомендуется часто менять места введения инсулина, пользоваться атравматичными иглами, очищенными препаратами новоинсулинов.
Новые технологии в диагностике и лечении СД
1. Обновление средств мониторинга глюкозы. Предполагается создание датчиков, работающих в спектре радиочастот, определителей сахара в тканевой жидкости путем ее подсоса с поверхности кожи при помощи полоскок специального лейкопластыря.
- Создание новых поколений инсулинов быстрого всасывания («мономерных инсулинов»), что уменьшает риск гипогликемии.
— Поиск новых методов введения инсулина. Прогнозируется отказ от инъекций ввиду перехода на неинвазивные формы инсулина — аэрозоли. Компьютеризированные насосы — подсадки позволят самому больному определить время и дозу очередного введения инсулина.
— Поиск заменителей инсулина. Циклоспорин — препарат, тормозящий первичный аутоиммунный ответ (тормозит продукцию ИЛ-2, ослабляет атаку антигенсодержащих клеток Т-хелперами, цитотоксичными Т-лимфоцитами, макрофагами).
При ИЗСД у детей циклоспорин в дозе 7,5 мг/кг (прием за завтраком и обедом) у 2/3 детей (средний возраст 10 лет) через 7 недель лечения позволяет обходится без инсулина, к 12 месяцам приема 3/4 больных вообще перестают нуждаться в инсулине.
— Трансплантация бета-клеток в печень (суспензия культуры бета-клеток вводится в воротную вену).
Доза экзогенного инсулина при этом снижается на 30%. Однако положительный эффект кратковременный (3-4 месяца), имеется опасность дополнительной иммунизации и аутоиммунного поражение собственной ПЖ. Предполагается подбор донорских клеток по НЛА системе (полная индентичность донора и реципиента) на фоне иммуносупрессивной терапии.
Диспансерное наблюдение при СД у детей
Осуществляется педиатром и эндокринологом и включает ведение на дому, обучение родителей и ребенка методам компенсации СД, периодические (каждые 6-12 месяцев) обследование и коррекция доз инсулина в эндокринологическом стационаре. Критериями эффективности являются нормализация показателей углеводного обмена, отсутствие ацидотических состояний и сосудистых осложнений, нормальные размеры печени, правильное половое и физическое развитие. Диспансерное наблюдение постоянное.
Прогноз при СД у детей., Профилактика СД у детей., Использованная литература
1. Л.М.Скордок, А.Ш.Стройкова Сахарный диабет. В кн.: Детские болезни (под ред. А.Ф.Тура и др.) — М., Медицина, 1985, с.526-534.
- В.Л.Лисс — Сахарный диабет. В кн.: Детские болезни (под ред. А. Ф. Шабалова).- СПб, СОТИС, 1993, с. 466-476.
- М.А.Жуковский Детская эндокринология.
— М., Медицина , 1982, с. 115-178.
- В.Г.Баранов, А.С.Стройкова — Сахарная диабет у детей. — М ., Медицина, 1980.
- Методические указания по циклу эндокринологии детского возраста (для студентов у курса ЛПМИ).
— Л., 1979.
- У.Мак-Моррей.- Обмен веществ у человека. — М., Мир, 1980.
- В.А.Михельсон, И.Г.Алмазова, Е.В.Неудахин — Коматозные состояния у детей.
— Л., Медицина, 1988, с. 99-114.
- Диспансерное наблюдение детей в поликлинике (под ред. К.Ф.Ширяевой).
— Л., Медицина, 1984, с. 226-237.
- Ю.А.Князев — Эпидемиология сахарного диабета у детей.
— Педиатрия, 1991, №2, с.7-10.
- Л.В.Арзамасцева, М.И.Мартынова — Социально-демографическая характеристика семей детей, больных сахарным диабетом. — Педиатрия, 1991, №2, с. 10-14.
- К.Д.Хусаинов и др.
— Активное выявление нарушений толерантности к глюкозе среди популяций с факторами рика по сахарному диабету. — Педиатрия , 1991, №2, с. 15-18.
- Л.Л.Вахрушева и др. — Роль тромбоксана А-2 и простоциклина в патогеннезе сахарного диабета у детей у детей и подростков. — Педиатрия, 1991, №2, с. 18-22.
- Д.Н.Исаев, С.М.Зелинская — “Внутренняя картина болезни” у детей с сахарным диабетом.
— Педиатрия, 1991. №2, с. 33-37.
- Препараты инсулина. Техника инъекций инсулина. — Педиатрия, 1989, №11, с.109-110.
- М.И.Балаболкин, А.Герасимов — Схемы назначения новоинсулинов.
— М., 1993.
- Лекарственные средства, созданные методом рекомбинантной ДНК. — Медикал Маркет, 1994, №2, с. 14-16.
- Человеческий инсулин — гумулин — его разнообразные формы.
— Медикал Маркет, 1994. №2, с. 16. 1
- Сахарный диабет: жестче контроль, слабее “вожжи”. — Медикал Маркет , 1994. №1, с. 22-24.
- Что достоверно известно о циклоспорине.
— Медикал Маркет, 1994, №1, с. 19-20.
- Инсулин лоспро. — Медикал Маркет, 1995, №3, с. 62-63.
- Дедов И.Н.
и др. — Как жить с диабетом . — ВЭНЦ АМН ССР, Москва, 1990.
- А.Древаль — Сахарный диабет, Диету выбирают двое. — Медицинская газета, 1993, №26, с. 8-9.
- Справочник — путеводитель практикующего врача.
2000 болезней от А до Я. — Под ред. И.Н.Денисова, Э.Г.Улумбекова. — М., ГЭОТАР, 1999. — С. 304-306.
- М.И.Балаболкин, В.М.Креминская — Сахарный диабет. — Эндокринология. Интернет. 1998.
- Бирте С.Ольсен, Хенрик Мортенсен — Практическое руководство по лечению детей и подростков с сахарным диабетом.
2001 — med.ru »» Фармацевтические компании »» Ново Нордиск »» ИЗСД (диабет I типа).
